标的公司: Arrowhead Pharmaceuticals Inc.(NASDAQ:ARWR)
Arrowhead Pharmaceuticals Inc.(ARWR)的合作伙伴Janssen Pharmaceuticals, Inc(强生公司杨森制药),在美国肝病研究协会(AASLD)年会肝脏会议上发表REEF-1的临床数据,REEF-1是一项不同联合方案的IIb期研究,包括JNJ-73763989(JNJ-3989)(曾用名:ARO-HBV),和/或JNJ-56136379(JNJ-6379)以及nucleos(t)ide analog (NA) 用于治疗慢性乙型肝炎病毒感染(CHB)。
JNJ-3989是一种针对所有乙型肝炎病毒(HBV)RNA的研究性小干扰RNA(siRNA),从而降低所有病毒蛋白的水平。JNJ-6379是一种研究性衣壳组装调节剂(CAM-N),通过诱导形成不含HBV DNA和RNA的非传染性病毒颗粒来抑制病毒复制。Arrowhead于2018年10月与Janssen签订了一份许可和合作协议,以开发和商业化JNJ-3989。
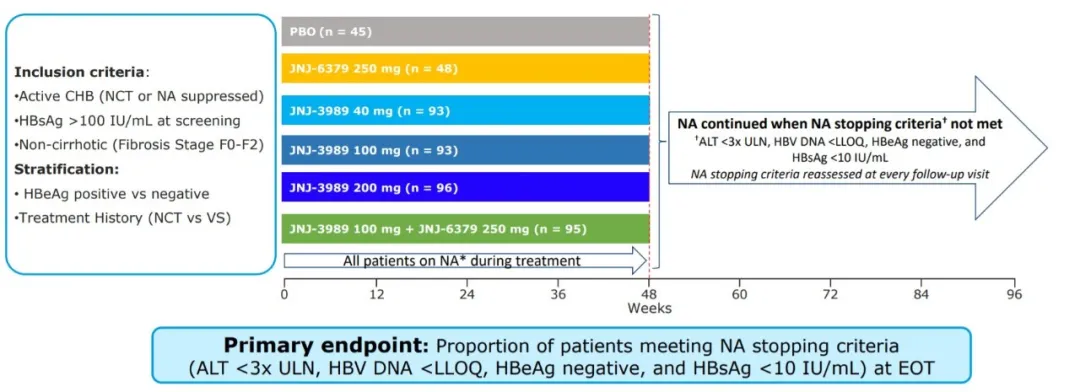
REEF-1(NCT03982186)是一项2b期、多中心、双盲、主动对照、随机研究,旨在评估JNJ-3989每月皮下注射48周(3种剂量水平分别为40、100和200mg)的疗效和安全性和/或对目前未治疗或病毒抑制的HBeAg阳性或阴性慢性乙型肝炎患者每日口服250毫克JNJ-6379联合每日口服NA。患者需要HBsAg水平大于100 IU/mL才能进入研究。所有研究组的平均基线HBsAg水平约为3.7 log10 IU/mL。研究的主要终点是治疗结束时(第48周)符合NA停止标准(ALT低于正常上限的3倍,HBV DNA低于定量下限,HBeAg阴性,HBsAg低于10 IU/mL)的患者比例。
标题:Efficacy and Safety of the siRNA JNJ-3989 and/or the Capsid Assembly Modulator (CAM) JNJ-6379 for the Treatment of Chronic Hepatitis B Virus Infection (CHB): Results from the Phase 2B REEF-1 Study
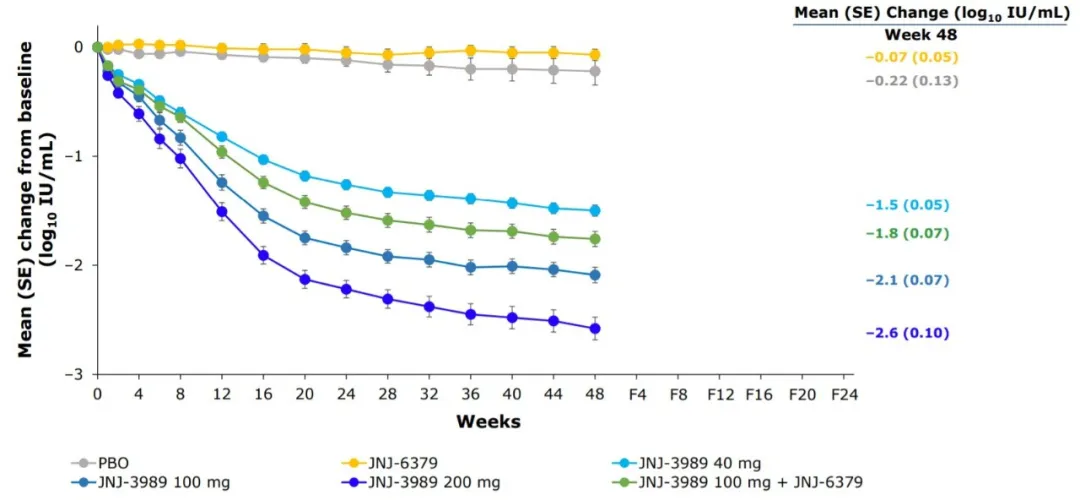
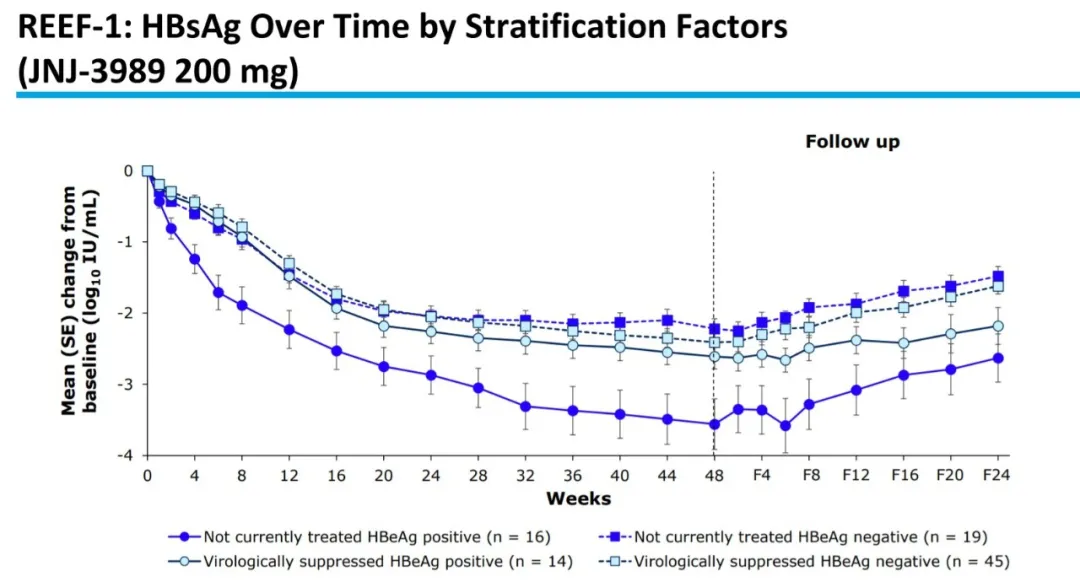
- JNJ-3989 200mg与NA队列的药效学反应(n=94)
- 在JNJ-3989 200mg NA队列中观察到HBsAg的最大减少
- 在其他队列中观察到剂量依赖性反应
- 在第48周,19.1%的患者符合NA停止标准
- 截至第72周,另有10.6%的患者符合NA停药标准,共29.7%
- 在第48周,HBsAg从基线检查时的平均减少量为2.6 log10
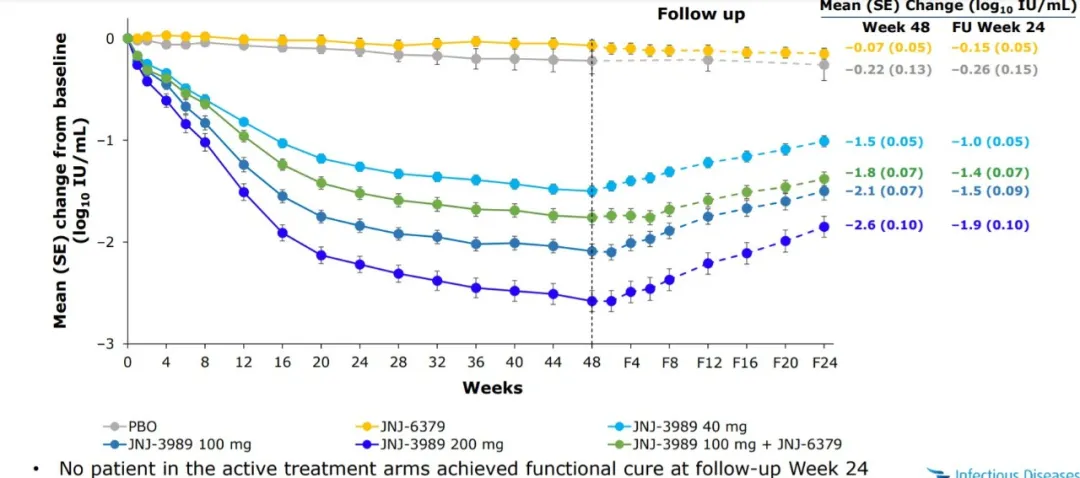
- 在第72周,HBsAg从基线检查时的平均减少量为1.9 log10
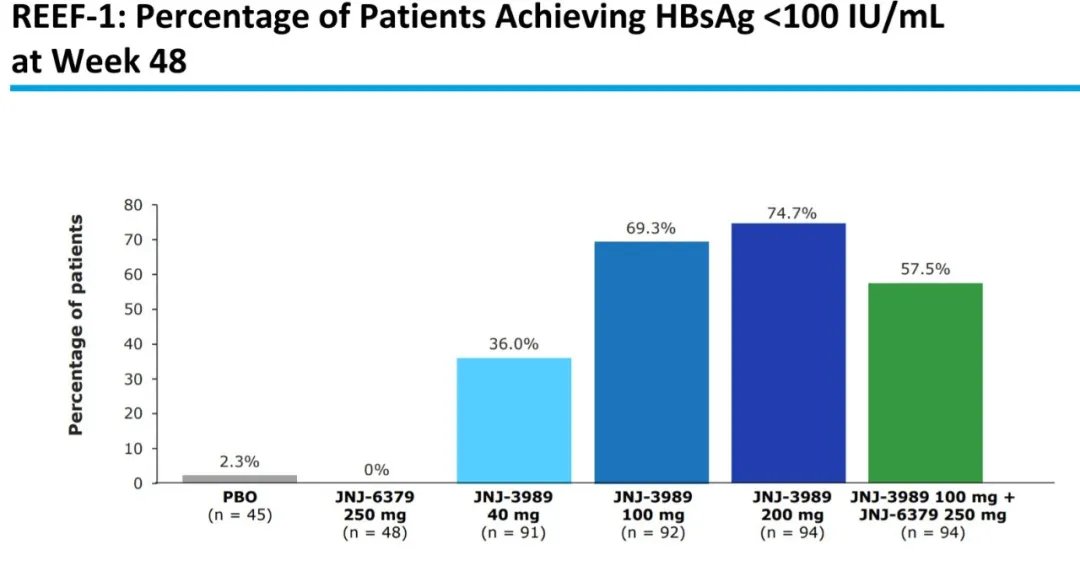
- 在第48周,74.7%的患者的HBsAg低于100 IU/mL
总结
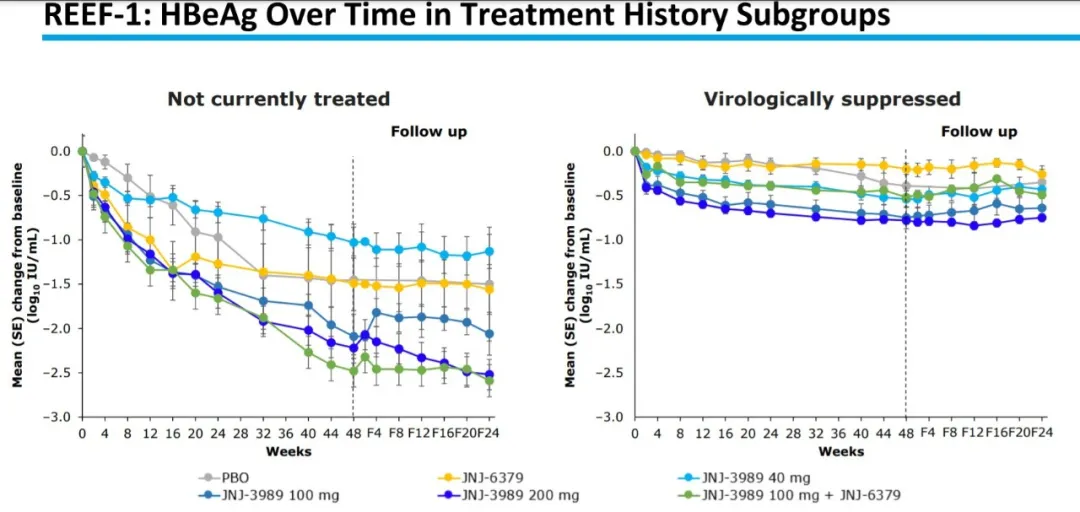
- 观察到剂量依赖性反应
- 第48周时,JNJ-3989 200mg(最高剂量)组:
- 19.1%的患者符合主要终点(NA停止标准),即HBsAg水平比基线水平降低最大(2.6 log10 IU/mL)
- 74.7%的患者达到HBsAg<100 IU/mL
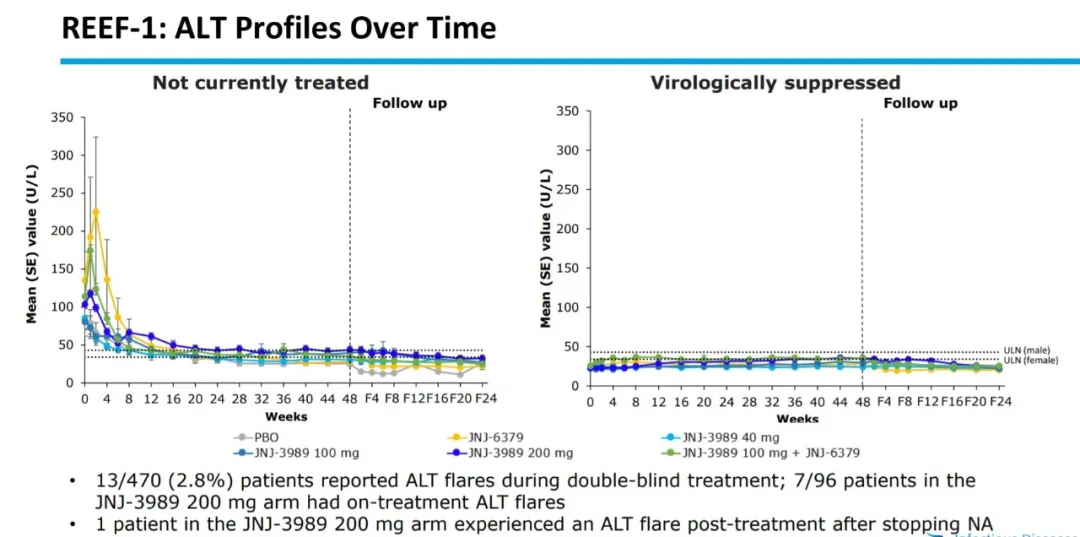
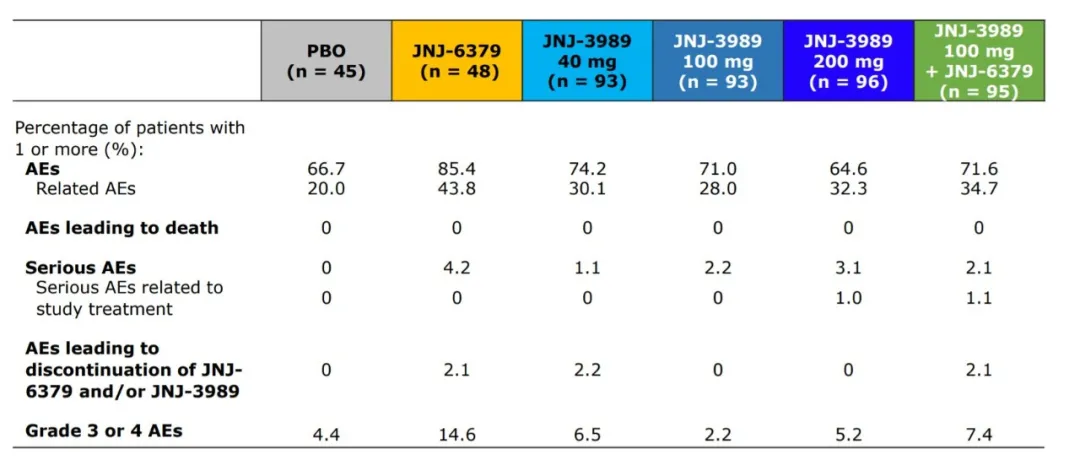
- 所有方案总体上耐受性良好,具有良好的安全性
- 目前正在进行涉及不同作用机制的联合研究
Arrowhead Pharmaceuticals Inc.
Arrowhead Pharmaceuticals Inc.通过沉默导致顽固性疾病的基因,开发出治疗顽固性疾病的药物。利用广泛的RNA化学组合和有效的传递方式,触发RNA干扰机制,诱导靶基因的快速、深入和持久敲除。RNA干扰,或称RNAi,是存在于活细胞中的一种机制,它抑制特定基因的表达,从而影响特定蛋白质的产生。Arrowhead基于RNAi的疗法利用了这种基因沉默的自然途径。
未经允许不得转载:美股开户者 » Arrowhead & Janssen: REEF-1慢性乙型肝炎感染IIb期临床数据
 美股开户者
美股开户者